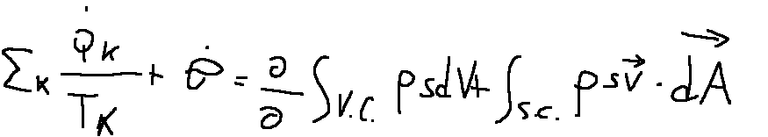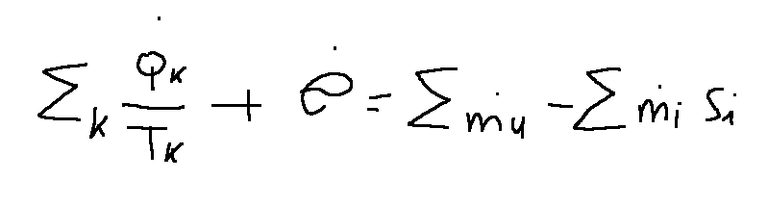
~~~ La versione in italiano inizia subito dopo la versione in inglese ~~~
ENGLISH
28-01-2024 - Physics - thermodynamics of open systems, second law [EN]-[IT]
Open systems thermodynamics, second law
Difference between closed and open systems
In short we can say that the difference between closed and open systems is a point that divides thermodynamics into two different phases, one more theoretical and the other more practical. For a long time, thermodynamics has dealt almost exclusively with closed systems, studying their equilibrium condition. Open systems, on the other hand, cannot reach a state of equilibrium, but they reach the state that is called "steady state" and in these systems there is a set of processes that act to maintain this steady state.
First law of thermodynamics for open systems
Recall the following from the first law of thermodynamics for open systems:
In an open system, energy can be exchanged in three different ways:
-1-Heat
Depending on temperature differences between system and environment
-2-Work
Depending on pressure differences between system and environment
-3-Mass flows
Following incoming mass flows that can exit and enter the system

WHERE:
Q = Heat
L = Work
ΔE = change in Energy
The Second Law of Thermodynamics for Open Systems
Recall that the second law of thermodynamics for closed systems states that the entropy associated with a control mass (M.C.) can vary over time due to the entropic flow due to exchanges of thermal power with the temperature reservoir and internal entropic production and external to the system.
Let's now talk about what the second law of thermodynamics states for open systems.
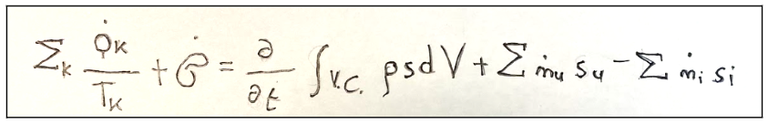
Here we follow the formula that represents the second law of thermodynamics for open systems
If we assume that we are in a stationary regime (a phenomenon in which certain quantities do not vary over time) and that the system has only one input and only one output we can derive the following formula
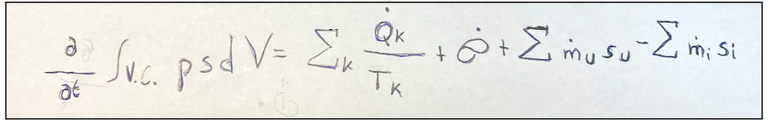
This means that the second law of thermodynamics of open systems states the following.
The change in entropy associated with a control volume over time depends on three causes:
-entropic flows associated with the thermal interaction between V.C. and particular devices, called SET, each of which is at a temperature Tk
-entropic production
-convective entropic flows, i.e. associated with the mass flows that pass through the S.C., at the entrance or exit.
Conclusions
The second law of open system thermodynamics states that the entropy associated with a control mass (M.C.) can vary over time due to entropic flow and entropic production.
Request
Have you ever tried to study or do exercises that concern the second law of thermodynamics for open systems?

28-01-2024 - Fisica - termodinamica sistemi aperti, seconda legge [EN]-[IT]
Termodinamica sistemi aperti, seconda legge
Differenza tra sistemi chiusi e aperti
In breve possiamo dire che la differenza tra sistemi chiusi e aperti è un punto che divide la termodinamica in due fasi diverse, uno più teorico e l’altro più pratico. A lungo la Termodinamica si è occupata quasi esclusivamente di sistemi chiusi, studiando la loro condizione di equilibrio. I sistemi aperti, invece, non possono raggiungere uno stato di equilibrio, ma raggiungono lo stato che viene chiamato “stato stazionario” e in questi sistemi esiste un insieme di processi che agiscono per mantenere questo stato stazionario.
Primo principio della termodinamica per i sistemi aperti
Ricordiamo quanto segue tratto dal primo principio della termodinamica per i sistemi aperti:
In un sistema aperto l’energia può essere scambiata attraverso tre diverse modalità:
-1-Calore
In funzione di differenze di temperatura tra sistema e ambiente
-2-Lavoro
In funzione di differenze di pressione tra sistema e ambiente
-3-Flussi di massa
A seguito dei flussi di massa in ingresso che possono uscire ed entrare nel sistema

DOVE:
Q = Calore
L = Lavoro
ΔE = variazione dell’Energia
La seconda legge della termodinamica per i sistemi aperti
Ricordiamo che la seconda legge della termodinamica per i sistemi chiusi afferma che l’entropia associata ad una massa di controllo (M.C.) può variare nel tempo a causa del flusso entropico dovuto agli scambi di potenza termica con il serbatoio di temperatura e della produzione entropica interna ed esterna al sistema.
Parliamo ora di ciò che afferma la seconda legge della termodinamica per i sistemi aperti.
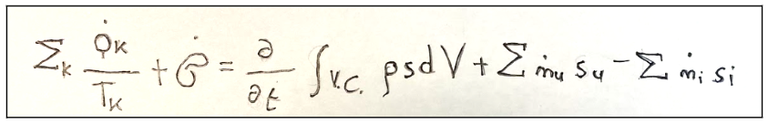
Qui si seguito la formula che rappresenta la seconda legge della termodinamica per i sistemi aperti
Se supponiamo di essere in un regime stazionario (fenomeno in cui determinate grandezze non variano nel tempo) e che il sistema ha un solo ingresso e una sola uscita possiamo ricavare la seguente formula

Questo significa che la seconda legge della termodinamica dei sistemi aperti stabilisce quanto segue.
La variazione nel tempo dell’entropia associata ad un volume di controllo dipende da tre cause:
-flussi entropici associati all’interazione termica tra V.C. e particolari dispositivi, detti SET, ciascuno dei quali si trova a temperatura Tk
-produzione entropica
-flussi entropici convettivi, associati cioè ai flussi di massa che attraversano, in ingresso o in uscita, la S.C..
Conclusioni
La seconda legge della termodinamica dei sistemi aperti stabilisce che l'entropia associata ad una massa di controllo (M.C.) può variare nel tempo a causa del flusso entropico e della produzione entropica.
Domanda
Avete mai provato a studiare o a fare esercizi che riguardano proprio la seconda legge della termodinamica per sistemi aperti?
THE END