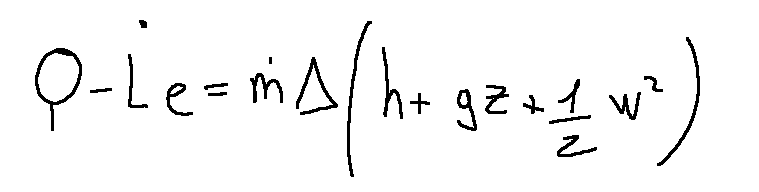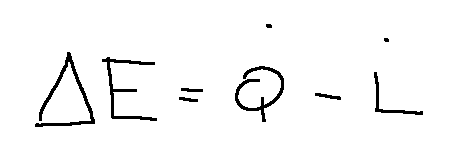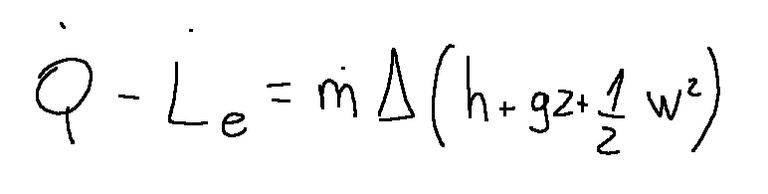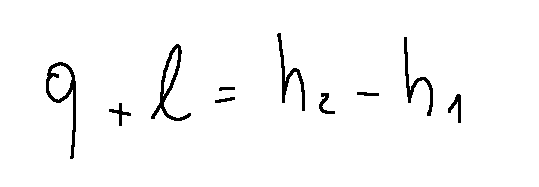~~~ La versione in italiano inizia subito dopo la versione in inglese ~~~
ENGLISH
27-01-2024 - Physics - Thermodynamics for open systems [EN]-[IT]
Thermodynamics for open systems
First law of thermodynamics - closed system
The first law of thermodynamics is also called the principle of conservation of energy. It states that, since energy can be neither created nor destroyed, the sum of the amount of heat transferred to a system and the work done on it must be equal to the increase in the internal energy of the system itself.
ΔU = Q - L
Where:
ΔU = change in internal energy
L = work. This is considered positive when it is effected by the system on the environment
Q = the heat. This is considered positive when it is provided by the environment to the system.
Open System
An open thermodynamic system is a region of space delimited by a boundary surface, within which the quantity of matter present can vary, i.e. there can be an exchange of matter between the system and the environment.
The first law of thermodynamics for open systems
The first law of thermodynamics for open systems states that the energy associated with a control mass (M.C.) can vary over time due to two different types of energy flows.
These two flows are thermal power and mechanical power.
The thermal power is identified with Q̇
The mechanical power is identified with L̇. For open systems, however, this is associated with two different mechanisms: mechanical propeller power (Le), mechanical thrust power Lp)
In an open system, the work L exchanged with the environment is the sum of the input, expulsion and useful work.
It can be assumed by hypothesis that the thermal energy received by the system is positive, the thermal energy released by the system is negative.
Regarding mechanical energy, if the system produces work
outward, this is good, but if the work is performed on the system, this is
negative.
The formula representing the first law of thermodynamics for open systems is the following
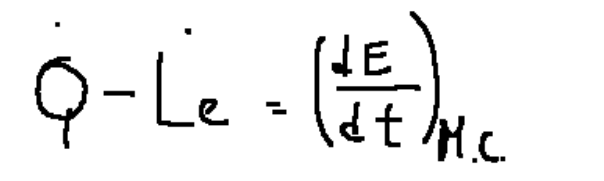
This formula is the same as the following
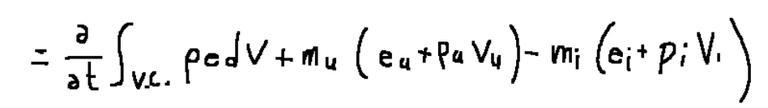
Conclusions
In conclusion, the first law of thermodynamics for open systems says that the energy associated with a control mass can vary due to two types of energy flows, thermal power and mechanical power.
Request
I find the thermodynamics of open systems much more complicated than that of closed systems, is it the same for you? Or are they understandable in the same way?

27-01-2024 - Fisica - Termodinamica per i sistemi aperti [EN]-[IT]
Termodinamica per i sistemi aperti
Primo principio della termodinamica - sistema chiuso
Il primo principio della termodinamica è detto anche principio di conservazione dell'energia. Esso afferma che, poiché l'energia non può essere né creata né distrutta, la somma della quantità di calore ceduta a un sistema e del lavoro compiuto sul medesimo deve essere uguale all'aumento dell'energia interna del sistema stesso.
ΔU = Q - L
Dove:
ΔU = variazione di energia interna
L = il lavoro. Questo è considerato positivo quando è effettuato dal sistema sull'ambiente
Q = il calore. Questo è considerato positivo quando è fornito dall'ambiente al sistema.
Sistema Aperto
Un sistema termodinamico aperto è una regione di spazio delimitata da una superficie di confine, all'interno della quale può variare la quantità di materia presente, cioè ci può essere scambio di materia tra il sistema e l’ambiente.
La prima legge della termodinamica per i sistemi aperti
La prima legge della termodinamica per i sistemi aperti afferma che l’energia associata ad una massa di controllo (M.C.) può variare nel tempo a causa di due differenti tipi di flussi energetici.
Questi due flussi sono la potenza termica e la potenza meccanica.
La potenza termica si identifica con Q̇
La potenza meccanica si identifica con L̇. Per i sistemi aperti però questa è associata a due diversi meccanismi: potenza meccanica d’elica (Le), potenza meccanica di pulsione Lp)
In un sistema aperto, il lavoro L scambiato con l’ambiente è la somma dei lavori di immissione, di espulsione e del lavoro utile.
Si può ammettere per ipotesi che l'energia termica ricevuta dal sistema sia positiva, l'energia termica ceduta dal sistema sia negativa.
Per quanto riguarda l'energia meccanica, se il sistema produce un lavoro
verso l'esterno, questo è positivo, se invece il lavoro viene eseguito sul sistema, questo è
negativo.
La formula che rappresenta la prima legge della termodinamica per i sistemi aperti è la seguente
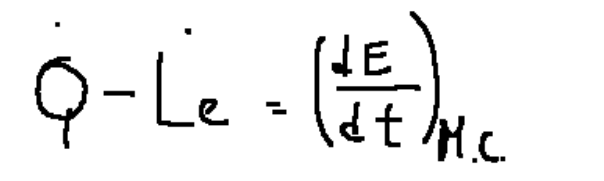
Questa formula è uguale alla seguente
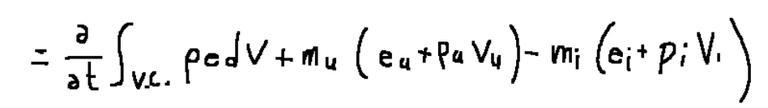
Conclusioni
In conclusione la prima legge della termodinamica per sistemi aperti dice che l'energia associata ad una massa di controllo può variare a causa di due tipi di flussi energetici, la potenza termica e la potenza meccanica.
Domanda
Io trovo la termodinamica dei sistemi aperti molto più complicata di quella dei sistemi chiusi, per voi è la stessa cosa? Oppure sono comprensibili allo stesso modo?
THE END